Die Schwerpunkte der Abteilung Foodborne Zoonoses liegen in der Verfahrensentwicklung und -validierung zum Nachweis relevanter Zoonose-Erreger, die in Verbindung mit Lebensmitteln tierischer Herkunft stehen. In der Vergangenheit kam es zum Beispiel durch den Verzehr von mit Listeria monocytogenes, Salmonellen oder Campylobacter spp. kontaminierten Produkten immer wieder zu lebensmittelbedingten Krankheitsausbrüchen. Das Ziel, Infektionen im Sinne des präventiven Verbraucherschutzes zu verhindern, kann nur dann erreicht werden, wenn eine frühe Erkennung mikrobieller Gefahren stattfindet. Aus diesem Grund beschäftigt sich die Abteilung Foodborne Zoonoses verstärkt mit der Entwicklung feldtauglicher Schnellverfahren, die idealerweise eine direkte Identifizierung von Pathogenen ermöglichen.
Im Hinblick auf einen schnellen Erregernachweis bietet die molekulare Diagnostik einen geeigneten Ansatz. Verfahren wie die Polymerase-Kettenreaktion (PCR) oder die Loop-mediated isothermal amplification (LAMP)-Methode weisen Pathogene auf der Basis einer spezifischen DNA-Vervielfältigung und mit hoher Empfindlichkeit nach. Die aufwändige und zeitintensive Kultivierung und Isolierung der Erreger entfallen daher in den meisten Fällen. Vor allem die LAMP-Methode lässt sich aufgrund der isothermalen Reaktionsbedingungen (konstante Reaktionstemperatur) mit nur minimalistischem Geräteaufwand umsetzen und eignet sich auch für die Durchführung unter eingeschränkten Bedingungen vor Ort.
Kurz gereifte Rohwürste stellen Risikolebensmittel dar und können eine Quelle für Infektionen mit Salmonellen und Listeria monocytogenes sein.

Salmonellen und Campylobacter werden am häufigsten in rohem Geflügelfleisch nachgewiesen. Infektionen können beispielsweise durch Kreuzkontaminationen während der Zubereitung von Nahrungsmitteln oder den Verzehr von unzureichend erhitztem Fleisch entstehen.
Impressionen aus dem Labor / Geräteübersicht:
Geräteübersicht
- LightCycler®96 (Roche Diagnostics International Ltd)
- Real-time-PCR
- 4-Kanal-Messung (Mulitplex)
- Schmelzkurvenanalyse
- Probendurchsatz: 96 pro Anwendung
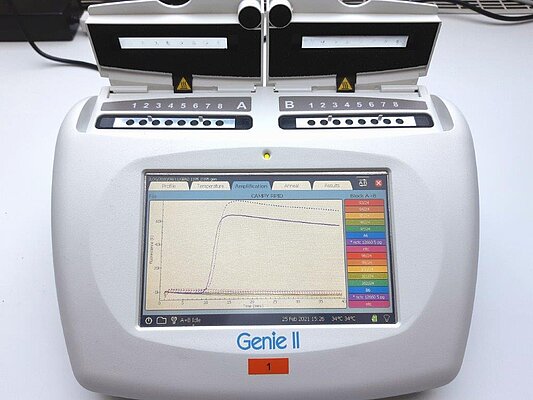
- Genie® II (OptiGene Ltd)
- Real-time LAMP Fluorometer
- 1-Kanal-Messung (Singleplex)
- Schmelzkurvenanalyse
- Genie® III (OptiGene Ltd)
- Real-time LAMP Fluorometer
- 2-Kanal-Messung (Multiplex)
- Schmelzkurvenanalyse
- ESEQuant TS2 (Qiagen)
- Real-time LAMP Fluorometer
- 6-Kanal-Messung (Multiplex)
- Schmelzkurvenanalyse
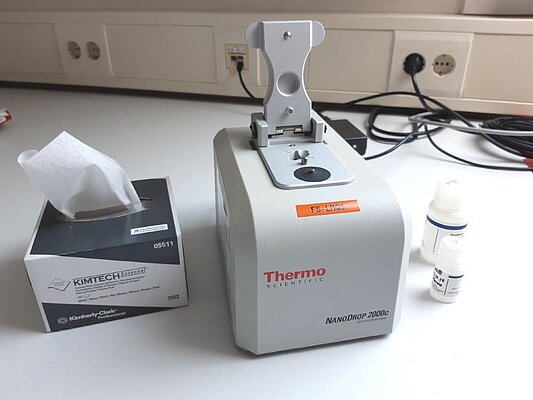
- NanoDrop 2000C (Thermo Scientific)
- UV-Vis Spektrophotometer
- Quantifizierung von DNA, RNA, Proteinen
- Reinheitsanalyse
- KingFisher Flex (ThermoFisher Sientific)
- Automatisierte Extraktion von DNA, RNA, Proteinen und Zellen
- Probendurchsatz: 96 pro Anwendung
- Maxwell® RSC Instrument (Promega) inkl. Quantus™ Fluorometer
- Automatisierte Extraktion von DNA und RNA
- integrierte DNA/RNA-Quantifizierung
- Precellys Evolution (Bertin Instruments)
- Zermahlen und Lyse biologischer Proben
- Homogenisieren schwieriger Proben wie Sporen, Knochen, Haaren usw.
- Schnelle Extraktion von DNA, RNA oder Proteinen